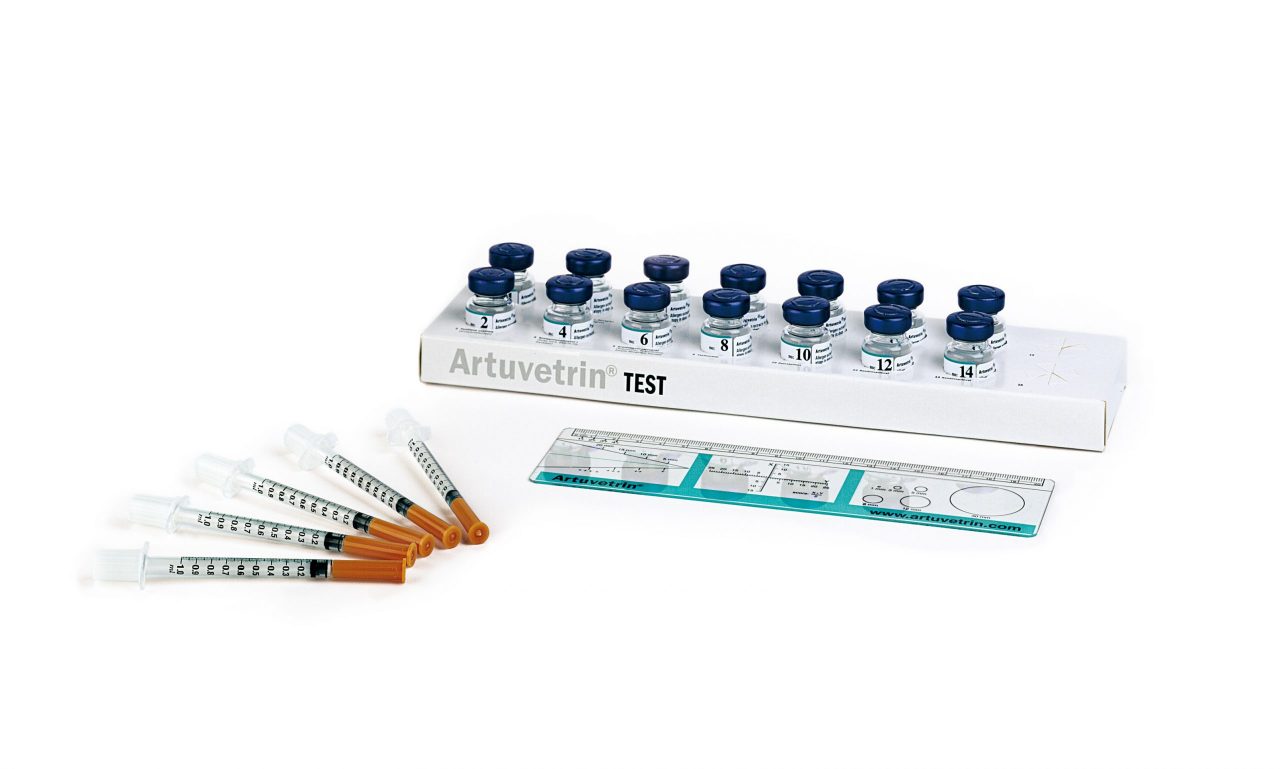
De Artuvetrin® Huidtest bepaalt voor welke stoffen een hond allergisch is, door kleine hoeveelheden van verschillende allergenen (subcutaan) in de huid te injecteren. Vervolgens is het mogelijk te beoordelen of er al dan niet een lokale reactie is opgetreden op de injectieplaats. Voordat de huidtest wordt uitgevoerd, moet het toedienen van eventuele medicatie die de resultaten kan beïnvloeden (waaronder prednison, , cyclosporine en antihistamine) 2–6 weken worden stopgezet.
Belangrijke feiten over de Artuvetrin® Huidtest
- 80 individuele allergenen of mengsels beschikbaar
- Geleverd in 3 ml flacons (voldoende voor 60 testen)
- 6 maanden houdbaar
- Levering binnen 8 werkdagen
- Concentraties op basis van vastgestelde drempelwaarden, voor betrouwbare uitslagen
Hoe u een huidtest uitvoert
De huidtest wordt uitgevoerd op de laterale thorax van de patiënt, nadat een stukje huid zorgvuldig is geschoren. Vervolgens worden een kleine hoeveelheid (0,05 ml) histamine en zoutoplossing (positieve en negatieve controles) plus oplossingen van de geselecteerde allergenen op verschillende locaties in de huid geïnjecteerd. Na 15–20 minuten worden alle injectieplaatsen beoordeeld op huidzwelling (vorming van een kwaddel). Indien sprake is van allergie voor een bepaalde stof zal een ontstekingsreactie verschijnen op de huid, zichtbaar als een zwelling. De uitbreiding van deze zwelling wordt vergeleken met die van de positieve en negatieve controles, waardoor het mogelijk is om vast te stellen waar de patiënt allergisch voor is. Een patiënt kan allergisch zijn voor allerlei stoffen.
Stappen van een huidtest
1. Scheer zorgvuldig een stukje huid op de laterale thoraxwand. De test kan alleen worden uitgevoerd op intacte huid.
2. Nummer de injectieplaatsen op de huid met een marker of pen met een tussenafstand van 2,5 cm.
3. Vul de spuiten met de verschillende allergeen- en controleoplossingen. De nummers op de flacons moeten corresponderen met die op de huid.
4. Spuit subcutaan 0,05 ml van elk allergeen en de controlevloeistoffen in (er verschijnt een bultje na injectie).
5. Stel na 15–20 minuten de huidreactie vast door de toename van de zwelling te labelen met een marker of pen.
Interpreteren van de huidtest
De huidreacties worden na 15–20 minuten gemeten en een eventuele toename van de zwelling wordt gemeten met een liniaal. De reactie op de negatieve controle is meestal 0 mm.
Kwaddels met een diameter van meer dan de helft van de diameter van de positieve controle worden als positieve resultaten beschouwd. (Dat wil zeggen de helft van de diameter van de positieve kwaddel min die van de negatieve kwaddel.) Bij de evaluatie van positieve reacties zijn niet alleen de grootte en de configuratie van de kwaddels van belang, maar is het ook belangrijk na te gaan of het specifieke allergeen relevant is binnen de voorgeschiedenis van de patiënt.
FAQ
1. Wat is de houdbaarheid van de Artuvetrin® Huidtest na het aanprikken van de flacon?
De houdbaarheid wordt bepaald door de stabiliteit van de allergenen. De specifieke houdbaarheidsdata zijn vermeld op elk etiket.
2. Wat is de wachttijd voor het uitvoeren van de Artuvetrin® Huidtest na behandeling met steroïden, cyclosporine of antihistamine?
Bepaalde diergeneesmiddelen kunnen interfereren met de huidtest. Minimaal twee weken (en bij depotpreparaten minimaal 6 weken) voorafgaand aan de allergietest dient elke medicatie met antihistaminica en glucorticosteroïden te worden stopgezet.1
1Olivery, et al. Evidence-based guidelines for anti-allergic drug withdrawal times before allergen-specific intradermal and IgE serological tests in dogs. Vet Derm 24 (2013) 225–232.
3. Welke typen sedatie kunnen worden gebruikt voor de Artuvetrin® Huidtest en welke niet?
Aangezien de huidtest in principe niet pijnlijk is, zijn analgetica (anesthetica) niet nodig. Sedatie is voldoende, maar het type sedatiemiddel moet zorgvuldig worden gekozen.
De middelen die geen invloed hebben op de uitslagen zijn:¹
- Xylazinehydrochloride (o.a. Sedazine)
- Medetomidine (o.a. Domitor)
- Tiletamine hydrochloride/zolazepam hydrochloride (o.a. Zoletil)
- Halothaan
- Isofluraan
De middelen die wel invloed hebben op de uitslagen zijn:
- Xylazinehydrochloride/ketamine hydrochloride
- Ketamine hydrochloride (o.a. Keta-ject)
- Diazepam
- Acepromaxinemaleaat (Neurotranq)
- Propofol
¹The ACVD Task Force on Canine Atopic Dermatitis (XVII): Intradermal testing. Vet Immun Immunopath 81 (2001) 289–304.
4. Hoe moet ik de Artuvetrin® Huidtest interpreteren wanneer de negatieve controle geen 0 mm is?
Bij een negatieve controle van meer dan 0 mm moet hiervoor gecompenseerd worden. Hiervoor kan de volgende formule worden gebruikt:
(Negatieve controle + positieve controle) / 2
Bijvoorbeeld:
- Negatieve controle: 6 mm
- Positieve controle: 14 mm
- (6 mm + 14 mm) / 2 = 10 mm
Alle resultaten groter dan of gelijk aan 10 zijn positief.
5. Welke medicatie kan worden gegeven zonder de uitslagen van de Artuvetrin® Huidtest en de serumtest te beïnvloeden?
Voor zover bekend kan de volgende medicatie worden gegeven aan honden of katten zonder de uitslagen te beïnvloeden:
- Oclacitinib
- Lokivetmab
- Antibiotica
- Antimycotica
- Medicatie tegen hartworm
- Vlooienbestrijdingsmiddelen
- Schildkliermedicatie
- Hartmedicatie
- NSAID’s
Dat wil zeggen dat deze medicatie gewoon kan worden toegediend.
6. Kunnen katten getest worden met de Artuvetrin® Huidtest en behandeld worden met Artuvetrin® Therapie?
De pathogenese van huidproblemen ten gevolge van een ongewenste reactie op omgevingsallergenen is bij katten grotendeels onbekend. Daarom is de betrouwbaarheid van de resultaten van huidtesten met allergenen bij katten niet geheel duidelijk. Het gebruik van immunotherapie bij katten wordt in verband gebracht met een duidelijke verbetering van klinische symptomen (60–70% van de katten vertoonde een verbetering)¹. Deze bevindingen worden ondersteund door de ervaring van enkele dierenartsen die immunotherapie toepassen bij katten.
¹Efficacy of hyposensitisation in feline allergic diseases based upon the results of in vitro testing for allergen-specific immunoglobulin E. J Amer Animal Hosp Assoc 33(3), 282–288.